Lý thuyết về dãy điện hoá kim loại chi tiết nhất
Dãy điện hoá kim loại là gì? Ý nghĩa của dãy điện hoá kim loại: So sánh tính oxi hoá khử, xác định chiều phản ứng oxi hoá khử, xét 1 phản ứng xảy ra hay không. Cách nhớ nhanh dãy điện hoá kim loại
Ở bài trước, ta đã tìm hiểu về các tính chất cơ bản của kim loại. Hôm nay, HocThatGioi sẽ cùng các bạn tiêp tục tìm hiểu về bài tiếp theo về kim loại – đó là bài Dãy điện hoá kim loại. Vậy thì dãy điện hoá là gì? Có ý nghĩa như thế nào? Làm sao để ghi nhớ được chúng lâu và chính xác nhất? Tất cả đã được HocThatGioi trình bày rất đầy đủ và chi tiết qua bài viết dưới đây nên các bạn cứ thoải mái tham khảo nhé!
1. Dãy điện hóa kim loại là gì?
Trong phản ứng hóa học, cation kim loại có thể nhận electron để trở thành nguyên tử kim loại và ngược lại, nguyên tử kim loại có thể nhường electron để tạo thành cation kim loại.
Cụ thể như:
- Cu^{2+} + 2e \leftrightarrow Cu.
- Ag^{+} + 1e \leftrightarrow Ag.
Tổng quát:
M^{n+} + ne \leftrightarrow M.
Dạng OXH \leftrightarrow Dạng khử
Dạng oxi hóa và dạng khử của cùng một nguyên tố kim loại tạo nên cặp oxi hóa – khử (M^{n+}/M).
Như vậy, dãy điện hóa của kim loại là dãy những cặp oxi hóa – khử của kim loại được sắp xếp theo chiều tăng dần tính oxi hóa của ion kim loại và giảm dần tính khử của kim loại.

2. Ý nghĩa dãy điện hóa kim loại
2.1 So sánh tính oxi hóa – khử
Tính oxi hóa của ion M^{n+} càng mạnh thì tính khử của kim loại M càng yếu và ngược lại (tính oxi hóa của ion M^{n+} càng yếu thì tính khử của kim loại M càng mạnh).
Cụ thể như:
- Kim loại Na có tính khử mạnh do đó ion Na^+ có tính oxi hóa yếu.
- Ion Ag^+ có tính oxi hóa mạnh do đó kim loại Ag có tính khử yếu.
2.2 Xác định chiều phản ứng oxi hóa – khử
Dãy điện hóa của kim loại cho phép dự đoán chiều của phản ứng giữa hai cặp oxi hóa – khử theo quy tắc alpha (α): Phản ứng giữa hai cặp oxi hóa – khử sẽ xảy ra theo chiều chất oxi hóa mạnh hơn sẽ oxi hóa chất khử mạnh hơn, sinh ra chất oxi hóa yếu hơn và chất khử yếu hơn.
Cách xác định chiều của phản ứng oxi hóa – khử theo quy tắc alpha: Giả sử có hai cặp oxi hóa khử: X^{x+}/ X và Y^{y+}/ Y (trong đó cặp X^{x+}/ X đứng trước cặp Y^{y+}/ Y trong dãy điện hóa). Xác định chiều của phản ứng oxi hóa khử.
Bước 1: Viết hai cặp oxi hóa – khử theo đúng thứ tự trong dãy điện hóa \frac{X^{x+}}{X} \frac{Y^{y+}}{Y}
Bước 2: Áp dụng quy tắc alpha (α)
Phản ứng xảy ra theo chiều mũi tên như sau:
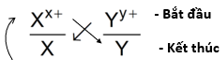
Bước 3: Xác định chiều phản ứng:
Phản ứng xảy ra như sau:
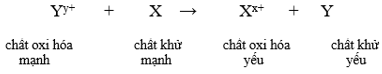
2.3 Xét một phản ứng oxi hóa – khử xảy ra hay không
Để xét một phản ứng oxi hóa – khử có xảy ra hay không cần nắm được quy tắc alpha: Chất khử mạnh + chất oxi hóa mạnh → chất oxi hóa yếu hơn + chất khử yếu hơn.
3. Cách nhớ nhanh dãy điện hoá kim loại
Dãy điện hoá kim loại rất dài và phức tạp, khó nhớ nhưng nếu bạn có thể biến tấu nó thành một đoạn thơ thì việc nhớ nó sẽ trở nên dễ dàng hơn:
Chẳng hạn như:
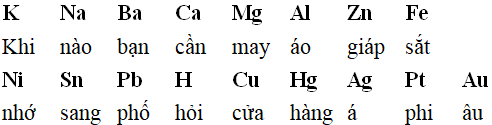
Hay có thể biến tấu rằng:
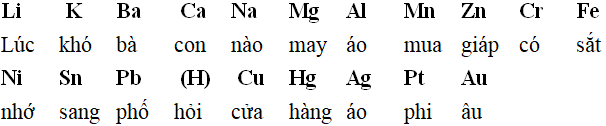
Hay để nhớ thêm vị trí của các cặp oxi hóa – khử của kim loại sắt có thể nhớ bằng biến tấu thành:

Bạn nào học tốt Văn thì có thể nhớ bài thơ sau: “Mấy lời về dãy điện hóa kim loại”
MẤY LỜI VỀ DÃY ĐIỆN HÓA KIM LOẠI
Dãy điện hóa O sau khử trước (1)
Phản ứng theo quy ước alpha
Nhưng cần phải hiểu sâu xa
Trước sau ý nghĩa mới là thành công
Kali, Can, Nát tiên phong
Ma, Nhôm, Man, Kẽm tiếp không chịu hèn
Sắt rồi Cô đến Niken
Thiếc, Chì dẫu chậm cũng liền theo chân
Hiđro, Đồng, Bạc, Thủy ngân,
Bạch kim, Vàng nữa chịu phần đứng sau.
Ba kim (loại) mạnh nhất ở đầu
Vào dung dịch muối nước đâu “hủy liền”.
Khí bay, muối lại gặp kiềm,
Đổi trao phản ứng là quyền chúng thôi.
Các kim loại khác dễ rồi,
Vào dung dịch muối trước thời đẩy sau.
Với axit, nhớ bảo nhau:
Khử được hát cộng (H+), phải đâu dễ dàng.
Từ Đồng cho đến cuối hàng,
Sau Hiđro đấy, chẳng tan chút nào.
Vài lời bàn bạc, đổi trao,
Vun cây “Vườn Hóa” vui nào vui hơn.
Các bạn hãy chọn cho mình cách nhớ nào cảm thấy phù hợp nhất nhé.
Cảm ơn các bạn đã theo dõi bài viết của HocThatGioi về Dãy điện hoá kim loại chi tiết nhất. Nếu các bạn thấy hay và bổ ích, hãy chia sẻ cho bạn bè của mình để cùng nhau học thật giỏi nhá. Đừng quên để lại 1 like, 1 cmt để tạo động lực cho HocThatGioi và giúp HocThatGioi ngày càng phát triển hơn nhé! Chúc các bạn học thật tốt!





