Lý thuyết kèm bài tập quá trình đẳng nhiệt và định luật Bôi-lơ-Ma-ri-ốt đầy đủ chi tiết nhất
Các bài tập lý thuyết và vận dụng quá trình đẳng nhiệt là một trong những nỗi lo sợ của nhiều học sinh THPT nói chung và học sinh lớp 10 nói riêng bởi đây là một kiến thức cơ bản nhưng rất quan trọng thường xuất hiện trong các đề thi THPT qua các năm. Biết được điều đó, hôm nay HocThatGioi sẽ gửi đến các bạn bài viết Lý thuyết kèm bài tập quá trình đẳng nhiệt và định luật Bôi-lơ-Ma-ri-ốt đầy đủ chi tiết nhất để bạn đọc có thể nắm vững nội dung này nhé!

I. Lý thuyết quá trình đẳng nhiệt và định luật Bôi-lơ-Ma-ri-ốt
1. Trạng thái và quá trình biến đổi trạng thái
- Trạng thái của một lượng khí được xác định bằng thể tích V, áp suất p và nhiệt độ tuyệt đối T. Ở mỗi trạng thái chất khí có các giá trị p, V và T nhất định gọi là các thông số trạng thái. Giữa các thông số trạng thái của một lượng khí có những mối liên hệ xác định.
- Lượng khí có thể chuyển từ trạng thái này sang trạng thái khác bằng các quá trình biến đổi trạng thái.
- Những quá trình trong đó chỉ có hai thông số biến đổi còn một thông số không đổi gọi là đẳng quá trình
2. Quá trình đẳng nhiệt
Quá trình đẳng nhiệt là quá trình biến đổi trạng thái khi nhiệt độ được giữ không đổi.
3. Định luật Bôi-lơ – Ma-ri-ốt
Phát biểu: Trong quá trình đẳng nhiệt của một lượng khí nhất định, áp suất tỉ lệ nghịch với thể tích.
Phát biểu cách khác: Ở nhiệt độ không đổi, tích của thể tích một khối lượng khí với áp suất của lượng khí đó là một đại lượng không đổi.
Hệ thức của định luật Bôi-lơ-Ma-ri-ốt:
hay
pV = hằng số
p là áp suất (Pa hoặc N/m^2)
V là thể tích (m^3)
4. Đường đẳng nhiệt
Định nghĩa: đường đẳng nhiệt là đường biểu diễn sự biến thiên của áp suất theo thể tích khi nhiệt độ không đổi
Dạng đường đẳng nhiệt:
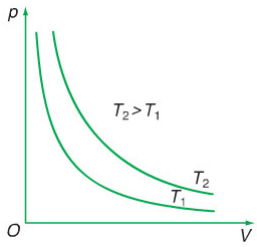
- Trong hệ tọa độ (p,V) đường đẳng nhiệt là đường Hypebol.
- Ứng với các nhiệt độ khác nhau của cùng một lượng khí có các đường đẳng nhiệt khác nhau.
II. Bài tập SGK quá trình đẳng nhiệt và định luật Bôi-lơ-Ma-ri-ốt
Bài 1 trang 159
Có 3 thông số trạng thái của một lượng khí:
1. Áp suất (P). Đơn vị áp suất: Paxcan (Pa); N/m^2; atmôtphe (atm); milimet thủy ngân (mmHg).
1 Pa = 1 N/m^2; 1 atm = 1,013.105 Pa; 1 atm = 760 mmHg.
2. Thể tích (V). Đơn vị : cm^3; lít ; m^3.
1 cm^3 = 10(-6) m^3; 1 lít = 1 dm^3 = 10(-3)(m^3)
3. Nhiệt độ tuyệt đối (T): Đơn vị : Kenvin kí hiệu K.
Liên hệ nhiệt độ kenvin và nhiệt độ cenciut: T = t + 273
Bài 2 trang 159
Quá trình đẳng nhiệt : Là quá trình biến đổi trạng thái của một lượng khí xác định, trong đó nhiệt độ được giữ không đổi
Bài 3 trang 159
Định luật Bôilơ-Mariốt : Trong quá trình đẳng nhiệt của một lượng khí nhất định, áp suất tỉ lệ nghịch với thể tích.
Hệ thức:
p \backsim \frac{1}{V}
hay
pV = hằng số
Bài 4 trang 159
Đường biểu diễn sự biến thiên của áp suất theo thể tích khi nhiệt độ không đổi gọi là đường đẳng nhiệt.
Trong hệ tọa độ (p, V) đường này là đường hypebol.
Bài 5 trang 159
Bài 6 trang 159
Bài 7 trang 159
Bài 8 trang 159

Bài 9 trang 159

Như vậy, bài viết về Lý thuyết kèm bài tập quá trình đẳng nhiệt và định luật Bôi-lơ-Ma-ri-ốt đầy đủ chi tiết nhất của HocThatGioi đến đây đã hết. Qua bài viết, hy vọng sẽ giúp các bạn tiếp thu được các kiến thức bổ ích. Đừng quên Like và Share để HocThatGioi ngày càng phát triển. Cảm ơn các bạn đã theo dõi hết bài viết





