Lý thuyết về Glucozơ đầy đủ chi tiết nhất
Tính chất vật lý và trangj thái tự nhiên của glucozơ, Cấu trúc phân tử, tính chất hoá học và điều chế, ứng dụng của glucozơ. Fructozơ-một đồng phân của glucozơ
Hôm nay, HocThatGioi sẽ cùng các bạn đi tìm hiểu về bài đầu tiên ở chương Cacbonhiđrat – Glucozơ. Bài viết này, HocThatGioi đã tổng hợp tất tần tật về lý thuyết của glucozơ rồi, từ tính chất vật lý, cấu trúc phân tử cho đến tính chất hoá học, điều chế,.. rất đầy đủ và vô cùng chi tiết. Vậy nên các bạn cứ tham khảo thoải mái nhé!
1. Tính chất vật lý và trạng thái tự nhiên Glucozơ
- Glucozơ là chất kết tinh, không màu, nóng chảy ở 146^oC (dạng α) và 150^oC (dạng β).
- Dễ tan trong nước.
- Có vị ngọt nhưng không ngọt bằng đường mía, Glucozơ có trong hầu hết các bộ phận của cây như lá, hoa, rễ, … và nhất là trong quả chín.
- Trong máu người có một lượng nhỏ glucozơ, hầu như không đổi (khoảng 0,1 %).
2. Cấu trúc phân tử Glucozơ
Glucozơ có công thức phân tử là C_6H_{12}O_6, tồn tại ở dạng mạch hở và mạch vòng.
2.1 Dạng mạch hở
Bằng thực nghiệm cho thấy:
- Khử hoàn toàn glucozơ thì thu được hexan. Vậy 6 nguyên tử C của phân tử glucozơ tạo thành 1 mạch hở không phân nhánh.
- Glucozơ có phản ứng tráng bạc, khi tác dụng với nước brom tạo thành axit gluconic, chứng tỏ trong phân tử có nhóm CH=O.
- Glucozơ tác dụng với Cu(OH)_2 tạo thành dung dịch màu xanh lam, chứng tỏ phân tử glucozơ có nhiều nhóm OH kề nhau.
- Glucozơ tạo este chứa 5 gốc CH_3COO, vậy trong phân tử có 5 nhóm OH.
Suy ra công thức phân tử glucozo dạng mạch hở:
- CH_2OH–CHOH–CHOH–CHOH–CHOH–CH=O.
- Hoặc viết gọn là:CH_2OH[CHOH]_4CHO
2.2 Dạng mạch vòng
Glucozơ kết tinh tạo ra hai dạng tinh thể có nhiệt độ nóng chảy khác nhau. Các dữ kiện thực nghiệm khác đều cho thấy hai dạng tinh thể đó ứng với hai dạng cấu trúc vòng khác nhau.
Nhóm –OH ở C_5 cộng vào nhóm C=O tạo ra hai dạng vòng 6 cạnh α và β:
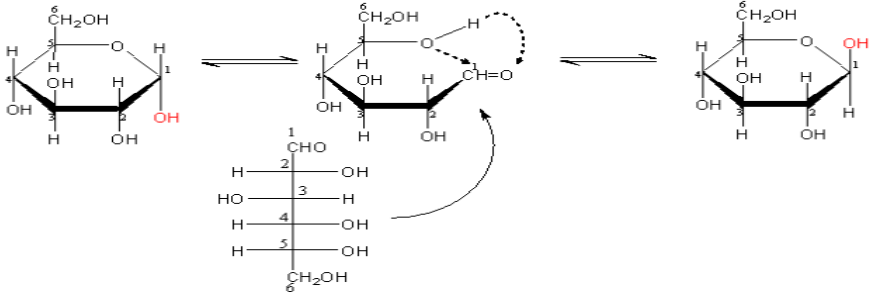
α – glucozơ (≈ 36 %) dạng mạch hở (0,003 %) β – glucozơ (≈ 64 %)
Nếu nhóm –OH đính với C_1 nằm dưới mặt phẳng của vòng 6 cạnh là α-, ngược lại nằm trên mặt phẳng của vòng 6 cạnh là β–
Nhóm–OH ở vị trí C_1 được gọi là OH– hemiaxetal
Để đơn giản, công thức cấu tạo của glucozơ có thể được viết như sau:
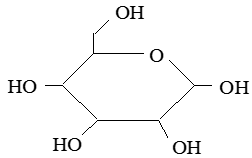
3. Tính chất hóa học
Glucozơ có các tính chất của anđehit và ancol đa chức
3.1 Tính chất của ancol đa chức (poliancol hay poliol)
Tác dụng với Cu(OH)2
Trong dung dịch, ở nhiệt độ thường glucozơ hòa tan Cu(OH)_2 cho dung dịch phức đồng – glucozơ có màu xanh lam:
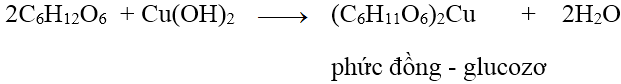
→ Phản ứng này chứng minh glucozo có nhiều nhóm OH
Phản ứng tạo este
Khi tác dụng với anhiđrit axetic, glucozơ có thể tạo este chứa 5 gốc axetat trong phân tử C_6H_7O(OCOCH_3)_5
CH_2OH(CHOH)_4CHO + 5(CH_3CO)_2O → CH_3COOCH_2(CHOOCCH_3)_4CHO + 5CH_3COOH→ Phản ứng này dùng để chứng minh trong phân tử glucozơ có 5 nhóm OH..
3.2 Tính chất của anđehit
Oxi hóa glucozơ
Với dung dịch AgNO_3 trong NH_3, đun nóng (thuốc thử Tollens) cho phản ứng tráng bạc
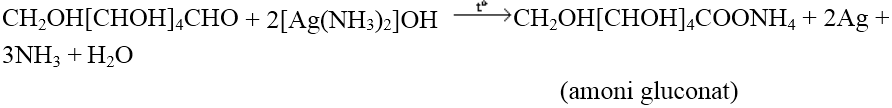
Với dung dịch Cu(OH)_2 trong NaOH, đun nóng (thuốc thử Felinh) Glucozo khử Cu (II) thành Cu (I) tạo kết tủa đỏ gạch Cu_2O.
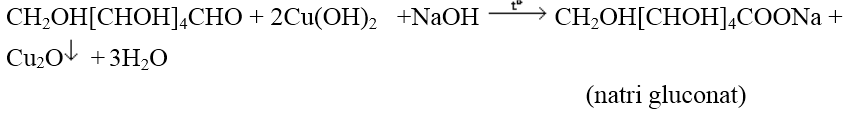
Với dung dịch nước brom:

→ Các phản ứng này chứng tỏ glucozơ có nhóm CHO.
Khử glucozơ
Khi dẫn khí hiđro vào dung dịch glucozơ đun nóng (xúc tác Ni), thu được một poliancol có tên là sobitol:
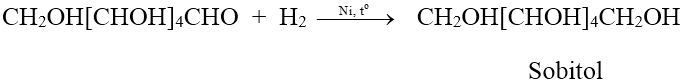
3.3 Phản ứng lên men
Khi có enzim xúc tác, glucozơ bị lên men cho ancol etylic và khí cacbonic:

3.4 Tính chất riêng của dạng mạch vòng
Riêng nhóm –OH ở C_1 (–OH hemiaxetal) của dạng vòng tác dụng với metanol có HCl xúc tác, tạo ra metyl glicozit:
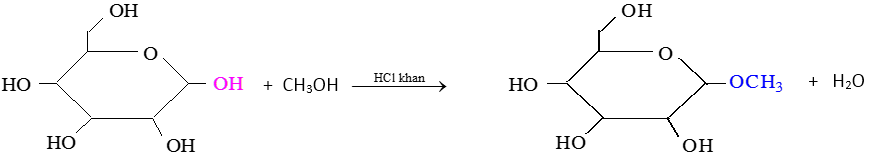
Khi nhóm –OH ở C_1 đã chuyển thành nhóm –OCH_3, dạng vòng không thể chuyển sang dạng mạch hở được nữa.
4. Điều chế, ứng dụng
4.1 Điều chế (trong công nghiệp)
- Thủy phân tinh bột với xúc tác là HCl loãng hoặc enzim.
(C_6H_{10}O_5)_n + nH_2O → nC_6H_{12}O_6
- Thủy phân xenlulozơ với xúc tác HCl đặc:
(C_6H_{10}O_5)_n +nH_2) → nC_6H_{12}O_6
- Thủy phân mantozo:
C_{12}H_{22}O_{11} + H_2O → 2C_6H_{12}O_6 (glucozơ)
- Thủy phân saccarozo:
C_{12}H_{22}O_{11} + H_2O → C_6H_{12}O_6 (glucozơ) +C_6H_{12}O_6 (fructozơ)
- Trùng hợp HCHO:
6HCHO → C_6H_12O_6 (Ca(OH)_2, t^o)
4.2 Ứng dụng
- Trong y học: dùng làm thuốc tăng lực cho người bệnh (dễ hấp thu và cung cấp nhiều năng lượng)
- Trong công nghiệp: dùng để tráng gương, tráng ruột phích (thay cho anđehit vì anđehit độc)
5. Đông phân của Glucozơ – Fructozơ
Fructozo là một đồng phân của glucozo
5.1 Công thức cấu tạo
- Công thức phân tử C_6H_{12}O_6.
- Công thức cấu tạo CH_2OH - CHOH - CHOH - CHOH - CO - CH_2OH.
- Trong dung dịch, fructozơ tồn tại chủ yếu ở dạng β, vòng 5 hoặc 6 cạnh.
5.2 Tính chất vật lí
- Là chất rắn kết tinh, dễ tan trong nước, có vị ngọt gấp rưỡi đường mía và gấp 2,5 lần glucozơ.
- Vị ngọt của mật ong chủ yếu do fructozơ (chiếm tới 40 %).
5.3 Tính chất hóa học
Fructozơ có tính chất của poliol và của OH – hemiaxetal tương tự glucozơ
Trong môi trường trung tính hoặc axit, fructozơ không thể hiện tính khử của anđehit, nhưng trong môi trường kiềm, fructozơ lại có tính chất này do có sự chuyển hóa giữa glucozơ và fructozơ qua trung gian là một enđiol.
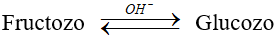
* Chú ý: Fructozơ không phản ứng được với dung dịch nước brom và không có phản ứng lên men.
Cảm ơn các bạn đã theo dõi bài viết của HocThatGioi về Lý thuyết về Glucozơ đầy đủ chi tiết nhất. Nếu các bạn thấy hay và bổ ích, hãy chia sẻ cho bạn bè của mình để cùng nhau học thật giỏi nhá. Đừng quên để lại 1 like, 1 cmt để tạo động lực cho HocThatGioi và giúp HocThatGioi ngày càng phát triển hơn nhé! Chúc các bạn học thật tốt!
Bài viết khác liên quan đến Lớp 12 – Hóa – Cacbohidrat
- Lý thuyết về Saccarozơ, tinh bột và xenlulozơ đầy đủ nhất
- Lý thuyết Cacbonhiđrat và dạng bài đốt cháy cacbohiđrat
- 20 câu trắc nghiệm lý thuyết cacbohiđrat hay gặp
- Phương pháp giải phản ứng tráng bạc hay nhất
- Dạng toán phản ứng lên men của glucozơ cực chi tiết
- Phản ứng thủy phân cacbohiđrat và bài tập áp dụng





